G2.4 Eliminasjon
Generelt
Hepatisk metabolisme og renal ekskresjon er de dominerende eliminasjonsveiene for legemidler. Clearance kan sees på som en proporsjonalitetsfaktor som beskriver hvor mye av legemidlet som fjernes per tidsenhet ved en gitt konsentrasjon i plasma, se figur G2.3. Kroppens totalclearance av et legemiddel er lik summen av clearance i de enkelte organer. Totalclearance gir dermed et mål på kroppens totale evne til å eliminere et legemiddel.
Hepatisk metabolisme
Hepatisk metabolisme er den viktigste eliminasjonsvei for lipidløselige legemidler og omfatter to hovedtyper av metabolisme: Fase 1-metabolisme og fase 2-metabolisme. Fase 1-metabolisme er en kjemisk omdannelse (oksidasjon, reduksjon eller hydrolyse) der de vanligste prosessene er hydroksylering og demetylering. Fase 2-metabolisme innebærer en konjugering med et annet molekyl (f.eks. glukuronsyre, acetat eller sulfat) og gir økt vannløselighet og vanligvis inaktivering, men i enkelte tilfeller også bevart eller økt aktivitet (f.eks. metabolisme av morfin til morfin-6-glukuronid).
Betydelig interindividuell variasjon i farmakokinetikk er knyttet til fase 1-metabolisme i cytokrom P450(CYP)-systemet. CYP-enzymene er en gruppe enzymer lokalisert til levercellenes mikrosomer og katalyserer omdannelse av en rekke endogene og eksogene stoffer. Enkelte CYP-enzymer kan utvise stor variasjon i aktivitet fra individ til individ pga. genetiske forskjeller, miljøpåvirkning (røyking, alkohol, kostholdsfaktorer), legemiddelinteraksjoner (enzyminduksjon eller -hemning), aldersbetingede variasjoner eller sykdomsbetinget variasjon (nedsatt leverfunksjon). 5–10 % av den kaukasiske befolkning har vesentlig redusert metabolismekapasitet via visse CYP-enzymer, fremfor alt CYP2C9, CYP2C19 og CYP2D6. Det finnes også andre enzymsystemer som utviser genetisk betinget variasjon. Noen slike er N-acetyltransferase-2 (metaboliserer f.eks. isoniazid og sulfonamider), pseudokolinesterase (metaboliserer suksameton), uridindifosfat-glykuronosyltransferase(UGT)-1A1 (metaboliserer irinotekan), UGT1A4 (metaboliserer lamotrigin) og tiopurin-metyltransferase (metaboliserer azatioprin og 6-merkaptopurin).
Biliær ekskresjon
Legemidler med så høy molekylvekt at de ikke vil bli skilt ut i nyrene, kan utskilles i gallen. Fordi galleveiene munner ut høyt oppe i tynntarmen, vil noe av det utskilte legemidlet kunne absorberes igjen lenger ned i tarmen. Konjugerte legemiddelmetabolitter som utskilles i gallen, som visse glukuronider (f.eks. etinyløstradiol-glukuronid), dekonjugeres av bakterier i tarmen og kan dermed absorberes på nytt (enterohepatisk kretsløp). Dette forlenger tiden legemidlet er i organismen.
Renal ekskresjon
Renal ekskresjon er den viktigste eliminasjonsvei for vannløselige legemidler med begrenset lipidløselighet og er et resultat av tre ulike delprosesser:
Glomerulær filtrasjon: Legemiddel løst i plasmavannet (og derved ikke bundet til plasmaproteiner som holdes tilbake av filtrasjonsbarrieren) filtreres med samme hastighet som plasmavannet.
Aktiv tubulær sekresjon: Sekresjon fra blod til tubuluslumen i proksimale tubuli foregår ved hjelp av to familier av spesifikke transportpumper: Legemidler som er svake syrer (f.eks. probenecid, penicillin og sulfonamider) pumpes ut via organiske aniontransportører (OAT). Legemidler som er svake baser (f.eks. trimetoprim og amfetamin) pumpes ut via organiske kationtransportører (OCT). Syrer kan konkurrere med hverandre om OAT-transporten og baser kan konkurrere med hverandre om OCT-transporten, men syrer og baser konkurrerer ikke med hverandre. Probenecid har høyere affinitet for OAT-transportørene enn mange andre syrer og kan dermed hemme sekresjonen av f.eks. penicillin. Se også G6 Interaksjoner G6 Interaksjoner.
Passiv tubulær transport foregår ved diffusjon over tubulusmembranen, med en hastighet som er avhengig av permeabilitet og konsentrasjonsgradient. Denne transporten kan i prinsipp foregå i begge retninger, men reabsorpsjonen av legemidler med høy lipidløselighet fra tubuli og tilbake til blodet er klart viktigst. Slike legemidler vil transporteres så raskt tilbake til blodbanen ved passiv diffusjon at selv filtrasjon og aktiv sekresjon ikke gir nevneverdig nettoutskillelse i urin. Legemidler med høy lipidløselighet vil derfor ikke elimineres i særlig grad ved renal ekskresjon, men må brytes ned i leveren til mer vannløselige metabolitter først. Ved forgiftning med svake syrer som acetylsalisylsyre kan alkalisering av urinen ved hjelp av natriumhydrogenkarbonat (bikarbonat) gitt intravenøst øke eliminasjonen ved at økningen i urin-pH øker ladningen til det sure stoffet i tubulusvæsken. Derved reduseres også reabsorpsjonen.
Kinetikktyper
1. ordens kinetikk.De fleste legemidler elimineres ved såkalt førsteordens kinetikk. Dette innebærer at eliminasjonsprosessenes hastighet er proporsjonal med legemiddelkonsentrasjonen, og at halveringstiden dermed er konstant. Etter avsluttet behandling vil konsentrasjonen synke til halvparten etter én halveringstid, til 25 % etter to halveringstider, til 12,5 % etter tre halveringstider osv. Etter fem halveringstider er det kun ca. 3 % igjen i kroppen, og for praktiske formål kan man da si at «alt» legemiddel er ute av kroppen.
0. ordens kinetikk.For enkelte legemidler er konsentrasjonene så høye at eliminasjonsprosessene er helt eller delvis mettet, slik at man nærmer seg en maksimal verdi for eliminasjonshastighet. Ved fullstendig metning av eliminasjonsprosessen faller konsentrasjonen med en fast verdi per tidsenhet. Dette gjelder f.eks. etanol (gjennomsnittlig fall på 0,15 promille per time). Dette kalles 0. (nullte) ordens kinetikk. Legemidler med 0. ordens kinetikk har derfor ikke noen fast halveringstid. Eksempler på slike legemidler er salisylat når acetylsalisylsyre brukes i høye (analgetiske) doser, fenytoin og teofyllin. Ved inntak av høyere doser enn normalt, f.eks. ved intoksikasjoner, kan konsentrasjonen av en rekke legemidler øke så mye at metning eller begynnende metning kan oppstå og halveringstidene blir uforholdsmessig lange.
Den type kinetikk som eliminasjonsprosessen følger, har vesentlig betydning for økningen av konsentrasjonen (akkumulasjon) av et legemiddel ved gjentatt, regelmessig dosering under vedlikeholdsbehandling.
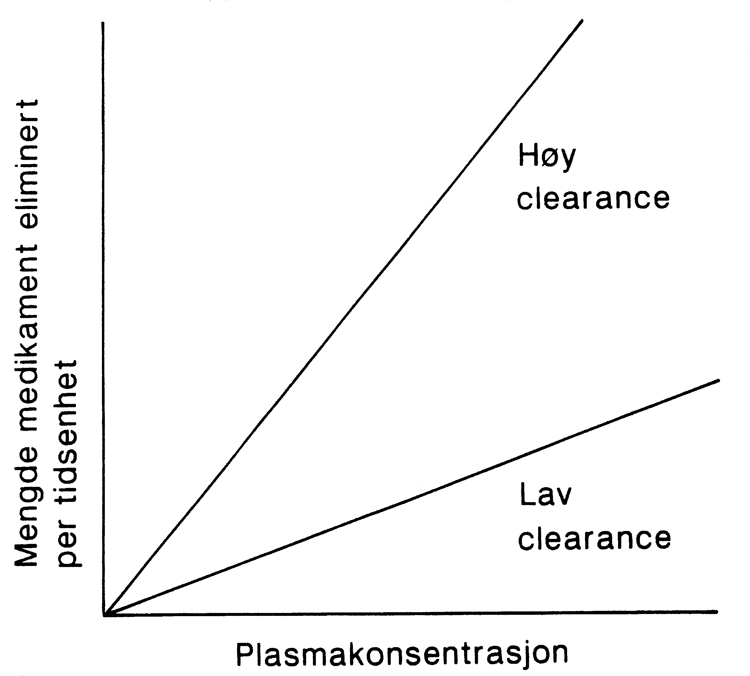
Figur G2.3 Legemiddeleliminasjon – clearance.
Ved førsteordens kinetikk er det en lineær sammenheng mellom mengden legemiddel som elimineres per tidsenhet (dX/dt) og plasmakonsentrasjonen (Cp) hvor clearance (Cl) representerer vinkelkoeffisienten: dX/dt = Cl × Cp. Ved en gitt plasmakonsentrasjon vil mengden som elimineres være langt større for et legemiddel med høy clearance enn for et legemiddel med lav clearance.